
Форуму 6621-й день
Текущая дата: Чт, 11 Июн 2026
|
Медицинский форум
КОМПАС ЗДОРОВЬЯ
управление в медицине
персональное и общественное здоровье
бесплатные консультации специалистов
не диагностика и лечение, но указание выбора правильного направления движения к оным
|
Источник вдохновения:
|
| Предыдущая тема :: Следующая тема |
| Автор |
Сообщение |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 2:55 am Заголовок сообщения: Введение в клиническую гемостазиологию Добавлено: Вс Янв 11, 2009 2:55 am Заголовок сообщения: Введение в клиническую гемостазиологию |

|
|
Введение в клиническую гемостазиологию
Баркаган З.С.
В данном пособии в максимально сжатой и доступной форме представлены данные об основных компонентах и механизмах функционирования системы гемостаза в норме и при наиболее часто встречающихся в практике врача патологических нарушениях в разных звеньях этой системы - при различных видах кровоточивости, ДВС-синдроме, тромбоэмболиях и тромбофилических состояниях.
Рассматриваются также принципы лабораторного контроля за гемостатической и антитромботической терапией. При этом предпочтение отдается наиболее доступным и вместе с тем достаточно информативным методам исследования.
Пособие рассчитано на практикующих врачей разных специальностей, поскольку геморрагии, тромбозы и ДВС-синдромы занимают одно из доминирующих мест в патологии человека.
СОДЕРЖАНИЕ
1. ОБЩИЕ СВЕДЕНИЯ О МЕХАНИЗМАХ И МЕТОДАХ ИССЛЕДОВАНИЯ СИСТЕМЫ ГЕМОСТАЗА
1.1. СОСУДИСТО-ТРОМБОЦИТАРНЫЙ ГЕМОСТАЗ
1.1.1. Тромбоциты и их роль в механизмах гемостаза
1.2. КОАГУЛЯЦИОННЫЙ ГЕМОСТАЗ
1.2.1. Трансформация фибриногена в фибрин
1.2.2. Трансформация протромбина в тромбин
1.2.3. Начальная фаза свертывания крови
1.2.4. Оценка результатов общих коагуляционных тестов
1.2.5. Витамин К-зависимые факторы свертывания крови
1.2.6. Неферментные факторы свертывания крови
1.3. ОСОБЕННОСТИ ФУНКЦИОНИРОВАНИЯ КОАГУЛЯЦИОННОГО КАСКАДА
1.4. ПРОТИВОСВЕРТЫВАЮЩИЕ МЕХАНИЗМЫ
1.5. ФИБРИНОЛИТИЧЕСКАЯ (ПЛАЗМИНОВАЯ) СИСТЕМА
2. МАРКЕРЫ АКТИВАЦИИ СИСТЕМЫ ГЕМОСТАЗА
2.1. МАРКЕРЫ АКТИВАЦИИ СОСУДИСТО-ТРОМБОЦИТАРНОГО ГЕМОСТАЗА
2.2. МАРКЕРЫ АКТИВАЦИИ СВЕРТЫВАЮЩЕЙ СИСТЕМЫ КРОВИ и ФИБРИНОЛИЗА
СПИСОК СОКРАЩЕНИЙ
| АГГ | - антигемофильный глобулин | РФМК | - растворимые фибринмономерные комплексы | | АДФ | - аденозиндифосфат | ТВ | - тромбиновое время | | АКТ | - аутокоагуляционный тест | ТПА | - тканевый плазминогеновый активатор | | АПТВ | - активированное парциальное тромбопластиновое время | ТСС | - тест склеивания стафилококков | | АТФ | - аденозинтрифосфат | ТЭЛА | - тромбоэмболия легочной артерии | | АЧТВ | - активированное частичное тромбопластиновое время | Фг | - фибриноген | | ВМК | - высокомолекулярный кининоген | ФМ | - фибрин-мономер | | ГП | - гликопротеин | ЭКГ | - электрокардиограмма | | ДВС-синдром | - синдром диссеминированного внутрисосудистого свертывания крови | РIVКА | - некарбоксилированные и нефункционирующие формы витамин К-зависимых факторов свертывания крови | | ПВ | - протромбиновое время | ТF | - тканевый фактор | | ПДФ | - продукты фибринолиза | ТFРI | - ингибитор тканевого пути свертывания |
|
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 3:10 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 3:10 am Заголовок сообщения: |

|
|
1. ОБЩИЕ СВЕДЕНИЯ О МЕХАНИЗМАХ И МЕТОДАХ ИССЛЕДОВАНИЯ СИСТЕМЫ ГЕМОСТАЗА
Биологическая система, обеспечивающая, с одной стороны, сохранение жидкого состояния циркулирующей крови, а с другой,
предупреждение и купирование кровотечений, обозначается как система гемостаза.
Это двуединство, казалось бы, противоположных, но необходимых для сохранения жизни организма функций предопределяет сопряженное участие в механизмах гемостаза различных морфологических структур и биохимических процессов, многоступенчатость их взаимодействия, функционирование на всех этапах механизмов самоускорения и самоторможения, активации и инактивации.
Наибольшее значение система гемостаза имеет для поддержания нормального кровотока и, вместе с тем, предупреждения и купирования кровотечений в тонкостенных и легко травмируемых сосудах малого калибра (до 100 мкм в диаметре). Поэтому от совершенства функционирования указанной системы в значительной степени зависят эффективность кровоснабжения тканей, предупреждение и купирование геморрагии, тромбозов, ишемий и инфарктов органов, защита от диссеминации бактерий и токсинов из очагов поражения по организму и т.д. Всем этим определяется важнейшее общебиологическое значение системы гемостаза и весьма существенная роль нарушений в ней в патогенезе подавляющего большинства заболеваний.
Гемостаз осуществляется тремя взаимодействующими между собой функционально-структурными компонентами:
- стенками кровеносных сосудов;
- клетками крови, в первую очередь, - тромбоцитами;
- плазменными ферментными (протеолитическими) системами -свертывающей, плазминовой (фибринолитической), калликреин-кининовой и комплемента.
Первыми в ответ на повреждение реагируют кровеносные сосуды и клетки крови (тромбоциты и, отчасти, эритроциты). Именно этой реакции принадлежит ведущая роль в предупреждении и остановке кровотечения из микрососудов. В связи с этим, сосудисто-тромбоцитарная реакция на повреждение обозначается как "первичный гемостаз", а процесс свертывания крови как "вторичный", хотя оба эти механизма взаимно индуцируют друг друга и функционируют на большом отрезке времени сопряженно.
1.1. СОСУДИСТО-ТРОМБОЦИТАРНЫЙ ГЕМОСТАЗ
В ответ на повреждение микрососуды отвечают спазмом, в результате чего капилляры и венулы временно запустевают и кровотечение из них в первые 20-30 секунд не возникает. Эта вазоконстрикция четко видна капилляроскопически при нанесении укола в ногтевое ложе. Она обусловлена рефлекторным сокращением гладкомышечных клеток сосудов и поддерживается вазоспастическими агентами, секретируемыми эндотелием и тромбоцитами - серотонином, тромбоксаном А2 и др. (см. далее). При некоторых видах сосудистой патологии (микроангиопатии, телеангиэктазии) эта локальная вазоспастическая реакция отсутствует, что легко выявляется капилляроскопически.
Функция эндотелия. В нормальных условиях эндотелий кровеносных сосудов обладает высокой тромборезистентностью и играет важную роль в поддержании жидкого состояния крови и предупреждении тромбозов. Это свойство эндотелия обеспечивается следующим: - контактной инертностью внутренней, обращенной в просвет сосуда поверхности этих клеток, в силу чего она не активирует системы гемостаза;
- синтезом мощного ингибитора агрегации тромбоцитов - простагландина I2 или простациклина;
- наличием на цитоплазматической мембране эндотелиальных клеток особого гликопротеина - тромбомодулина, связывающего тромбин, благодаря чему последний утрачивает способность вызывать свертывание крови, но сохраняет активирующее действие на систему двух важнейших антикоагулянтов -протеинов С и S;
- высоким содержанием на внутренней поверхности кровеносных сосудов мукополисахаридов и фиксацией на эндотелии комплекса "гепарин-антитромбин III";
- способностью стимулировать фибринолиз путем синтеза и секреции тканевого активатора плазминогена (ТПА), а также через систему "протеины С+S" (см. далее);
- элиминацией из крови активированных факторов свертывания крови и их метаболитов.
Вместе с тем, эндотелий обладает уникальной способностью менять свой антитромботический потенциал на тромбогенный. Такая трансформация происходит при застое крови, гипоксии, повреждении стенок сосудов физическими и химическими агентами, под влиянием экзо- и эндотоксинов, среди которых главенствующую роль играют бактериальные эндотоксины, иммунные комплексы, антиэндотелиальные и антифосфолипидные антитела, медиаторы воспаления (интерлейкины, фактор некроза опухоли и др.), а также клеточные и плазменные протеазы (эластаза, трипсин, тромбин и др.). Такая же трансформация наблюдается и при метаболических изменениях сосудистой стенки (атеросклероз, диабетическая ангиопатия).
Свойства субэндотелия. При гибели эндотелиальных клеток обнажается субэндотелий, содержащий большое количество коллагена, в контакте с которым происходят активация, адгезия и распластывание тромбоцитов, а также активация системы свертывания крови. Этот процесс реализуется при участии крупномолекулярных гликопротеинов, в первую очередь, фактора Виллебранда, фибронектина и фибриногена. Важная роль указанного механизма подтверждается тем, что при генетически обусловленных дефектах субэндотелия - истончении и обеднении его коллагеном (болезнь Рендю-Ослера, мезенхимальные дисплазии), как и при дефиците фактора Виллебранда, наблюдаются профузные и длительные кровотечения из поврежденных микрососудов. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 3:22 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 3:22 am Заголовок сообщения: |

|
|
1.1.1. Тромбоциты и их роль в механизмах гемостаза
Тромбоциты продуцируются в органах кроветворения гигантскими полиплоидными клетками - мегакариоцитами, от цитоплазмы которых они отшнуровываются в виде округлых или овальных плоских дисков диаметром от 2 до 4 мкм. В норме основным источником тромбоцитов служат зрелые, богатые зернистостью, мегакариоциты, но при необходимости интенсивного воспроизводства их (например, при большой убыли из крови под влиянием антитромбоцитарных антител или при потреблении в процессе массивного свертывания крови) происходит отшнуровка частиц от более молодых клеток мегакариоцитарного ряда, в результате чего в циркуляции появляются крупные с базофильной цитоплазмой и незначительной зернистостью клетки (так называемые "большие голубые пластинки").
Продолжительность жизни тромбоцитов человека составляет 7-10 дней. После выхода из костного мозга они циркулируют в крови и частично депонируются в селезенке и печени (около 20-25% всех клеток), откуда происходит вторичный их выход в кровоток. При гепатоспленомегалиях и портальном синдроме количество депонируемых тромбоцитов может резко возрастать и содержание этих клеток в крови воротной вены намного превышает их количество в периферической циркуляции (Я.А. Макаревич).
В крови здоровых людей содержится 170-350х109/л тромбоцитов. Уменьшение их количества ниже 80x109/л способствует появлению кровоточивости, риск которой резко возрастает при уровне ниже 20x109/л, а увеличение выше 800x109/л создает угрозу развития тромбозов.
Однако эти цифры условны, поскольку важны качественный состав циркулирующих в крови тромбоцитов, наличие в крови ингибиторов их функции, выраженность нарушений в других звеньях системы гемостаза и т.д. Так, при аутоиммунной тромбоцитопении угроза серьезной кровоточивости часто возникает лишь при содержании этих клеток в крови ниже 10-20х109/л, тогда как при ДВС-синдроме из-за наличия комплексных нарушений в системе гемостаза тяжелая кровоточивость может существенно усиливаться снижением числа тромбоцитов в крови до 80-100x109/л.
Участие тромбоцитов в гемостазе определяется следующими их функциями: - ангиотрофическоп, т.е. способностью поддерживать нормальную структуру и функцию стенок микрососудов, в том числе жизнеспособность и репарацию эндотелиальных клеток;
- способностью поддерживать спазм поврежденных сосудов путем секреции (высвобождения) вазоактивных веществ - серотонина, катехоламинов, бета-тромбомодулина и др., содержащихся в плотных и альфа-гранулах тромбоцитов;
- способностью образовывать в поврежденном сосуде тромбоцитарную пробку, что обеспечивается процессами адгезии этих клеток к субэндотелию и образованием их агрегатов, т.е. соединением друг с другом активированных тромбоцитов;
- участием тромбоцитарных факторов в процессе свертывания крови и в регуляции фибринолиза;
- стимуляцией процесса репарации в местах повреждения сосудистой стенки выделяющимся из подвергшихся адгезии тромбоцитов ростовым фактором, который является стимулятором размножения и перемещения гладкомышечных клеток и эндотелия, образования коллагена.
Тромбоцит окружен двухслойной фосфолипидной мембраной, в которую встроены рецепторные гликопротеины (ГП), взаимодействующие со стимуляторами (агонистами) адгезии и агрегации этих клеток. Из мембранных ГП наиболее важны ГП Iв, взаимодействующий с фактором Виллебранда и коллагеном, и ГП IIв/IIIa, связывающиеся с АДФ, адреналином и другими агонистами агрегации.
В процессе активации тромбоцитов меняются свойства этих рецепторов. Так, например, возрастает способность ГП IIв/IIIа соединяться с фибриногеном с образованием между клетками фибриногеновых и фибриновых мостиков.
К мембране тромбоцита прилегает аморфный белковый слой, имеющий толщину 15-20 нм, получивший название "плазматической атмосферы" или "гликокаликса". Этот слой отличается более высоким, чем в плазме, содержанием ряда белков, в том числе факторов свертывания крови, транспортируемых тромбоцитами в места остановки кровотечения.
Цитоплазматическая мембрана тромбоцитов образует множество проникающих вглубь клетки каналов с наружными выходами в виде узких устий. В силу этого, "плазматическая атмосфера" не только окружает эти клетки, но и проникает внутрь их, чем тромбоцит уподобляется губке.
Из внутренних органелл тромбоцитов (рис.1) в функциональном отношении наиболее важны система микротрубочек, содержащих сходный с актомиозином сократительный белок и гранулярный аппарат, от которого в значительной степени зависит гемостатическая функция этих клеток. Из этих гранул наиболее важны безбелковые гранулы высокой плотности, содержащие АТФ, АДФ, серотонин, катехоламины и другие вещества, необходимые для реализации гемостатической функции тромбоцитов, и белковые альфа-гранулы, в состав которых входят бета-тромбоглобулин, антигепариновый фактор (4-й пластиночный фактор), фактор Виллебранда, фибриноген, фактор V свертывания, ростовой фактор и др.

При активации тромбоцитов содержимое этих гранул выходит из клеток (реакция высвобождения) и играет важную роль в процессе агрегации и образования в сосуде гемостатической пробки. При качественных дефектах тромбоцита (тромбоцитопатиях) многие виды кровоточивости обусловлены отсутствием либо нарушением "реакции высвобождения" этих гранул.
Адгезивно-агрегационная функция тромбоцитов в значительной степени зависит от транспорта ионов кальция в эти клетки, а также от образования из мембранных фосфолипидов арахидоновой кислоты и циклических производных простагландинов (рис.2). При этом, в самих тромбоцитах образуется мощный стимулятор агрегации и ангиоспазма - тромбоксан А2, а в эндотелиальных клетках - антиагрегант и вазодилятатор - простациклин (РGI2). При повреждениях эндотелия в последнем также начинает преобладать образование тромбоксана. Этот дисбаланс между тромбоксаном и простациклином резко усиливает агрегацию и реакцию высвобождения гранул.
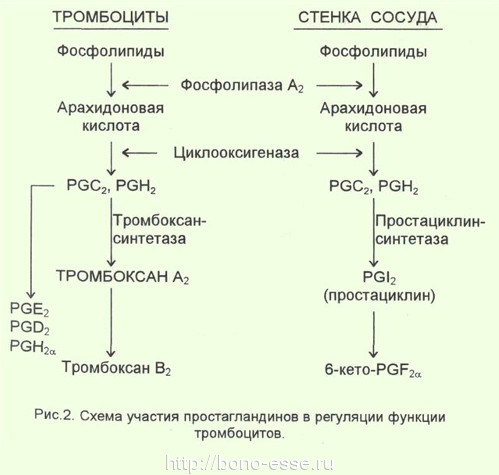
Основными стимуляторами адгезивно-агрегационной функции тромбоцитов являются турбулентное движение крови в зоне поражения или стенозирования сосудов, коллаген, АДФ, адреналин, тромбоксан А2, серотонин, а главным кофактором адгезии тромбоцитов к субэндотелию - фактор Виллебранда - мультимерный гликопротеин, входящий в состав комплекса фактора VIII (антигемофильного фактора свертывания; см. ниже). Имеется также ряд плазменных белков и пептидов, являющихся кофакторами или, наоборот, ингибиторами процесса агрегации. Для реализации этого процесса необходимы также ионы Са и Мg.
В целом, динамика адгезии и агрегации тромбоцитов схематически суммирована на рис.3.

Регистрация процесса агрегации тромбоцитов осуществляется с помощью специальных приборов - агрегометров. При воздействии малых доз агонистов агрегации (например, адреналина, низких концентраций АДФ) на агрегатограмме регистрируется двойная волна агрегации (рис.4): первая под влиянием введенного в плазму извне стимулятора, вторая - за счет реакции высвобождения собственных агонистов, содержащихся в гранулах тромбоцитов.
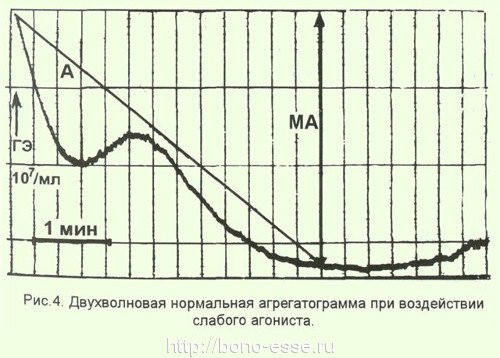
Вводимые извне большие дозы агонистов приводят к слиянию первой и второй волн агрегации. При отсутствии в тромбоцитах гранул или нарушении реакции их высвобождения начальная агрегация, вызванная введением извне агониста, сменяется дезагрегацией (рис.5). При отсутствии или блокаде мембранных рецепторов (например, при тромбастении Гланцманна) на агрегатограмме этот процесс вообще не регистрируется.
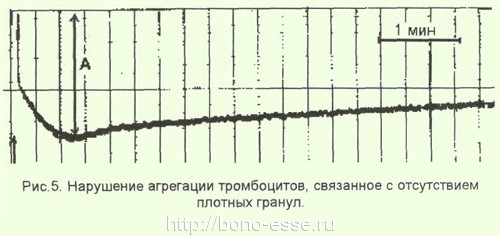
При значительных нарушениях адгезивно-агрегационной функции тромбоцитов возрастает время кровотечения из проколов или насечек кожи, что регистрируется с помощью пробы Дьюка, при которой остановка кровотечения происходит через 2-4 минуты после прокола кожи стандартным ланцетом у края мочки уха глубиной 3,5 мм но более точно - по определению времени и объема кровотечения из проколов на ладонной поверхности предплечья на фоне венозного стаза, вызванного сдавлением плеча манжетой для измерения АД и поддержания давления в ней на уровне 40 мм рт.ст. - проба Айви. В этой пробе остановка кровотечения при нормальной функции тромбоцитов происходит в первые 6 минут. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 4:16 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 4:16 am Заголовок сообщения: |

|
|
1.2. КОАГУЛЯЦИОННЫЙ ГЕМОСТАЗ
Свертывание крови - многоступенчатый (каскадный) ферментный процесс, в котором участвуют белки-протеазы, неферментные белковые акцелераторы процесса и конечный субстратный белок - фибриноген.
Перечень и принятая нумерация основных факторов свертывания, продолжительность их полужизни в циркуляции после внутривенного введения, а также необходимые для обеспечения гемостаза минимальные концентрации или активность этих белков приведены в табл.1.
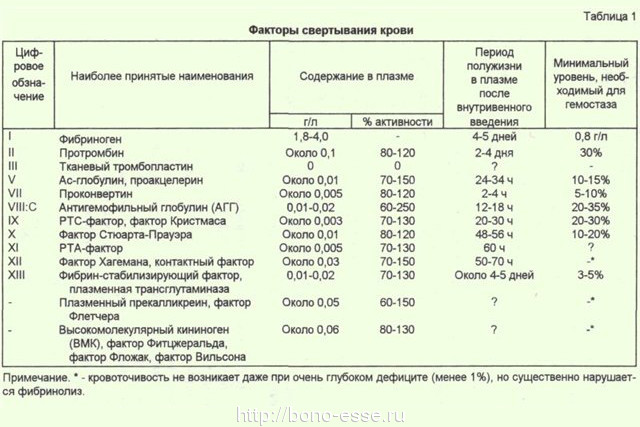
Для обозначения активированных факторов свертывания к их номеру добавляют букву "а", реже - букву "f", если активным действующим началом становится один из фрагментов фактора (например, фактор II - протромбин, фактор IIa - тромбин и т.д.).
Важной особенностью гемокоагуляционного каскада является то, что активация и взаимодействие факторов свертывания крови почти на всех этапах процесса происходят на свободных плазменных фосфолипидных мембранах (Д.М. Зубаиров, 1977, 1980; А.Ш. Бышевский и др., 1990; F. Jоbin, М.Р. Еsnouf, 1967; Н.С. Неmker et al., 1967; J.Р. Wu et al., 1993). Такой способностью к фиксации и активации факторов свертывания обладают только обращенные к наружной стороне мембраны головки отрицательно заряженных фосфолипидов - фосфатидилсерина, фосфатидилэтаноламина и др.
Показано, что ряд видов гиперкоагуляции связан с избытком в плазме крови фосфолипидных мембран, причем удаление последних без каких-либо других воздействий позволяет переводить повышенную свертываемость крови в пониженную (А.Ш. Бышевский и др., 1990; Z.S. Ваrkagan et al., 1992, 1995).
На рис. 6 приведена упрощенная каскадно-комплексная схема свертывания крови, в которой в рамки взяты процессы, реализуемые на фосфолипидных мембранах. Как и другие плазменные протеолитические системы, свертывание крови может функционировать по двум механизмам: - внутреннему, в котором наблюдается последовательная активация факторов XII, XI, IX+VIII, X+V и II;
- по внешнему (быстрому), который запускается поступлением в кровь извне тканевого фактора (фактор III или ТF), в состав которого входит апопротеин III и фосфолипид. ТF+фактор VIIа образуют активный комплекс, под влиянием которого активируются в присутствии ионов кальция и фосфолипидных мембран Х+V и II. Активированный фактор X не только переводит протромбин (фактор II) в тромбин (фактор IIа), но ретроградно активирует комплекс ТF-фактор VIIа.

Оба пути, как видно из схемы (рис.6), замыкаются на факторе X, вслед за чем они смыкаются и вплоть до образования фибрина сливаются в единый поток. Однако внешний и внутренний механизмы начального этапа свертывания крови не обособлены полностью друг от друга. Они взаимодействуют между собой путем взаимной активации факторов XII и VII, VII и IX.
При гиперлипидемиях отмечается частичная предактивация фактора VII и этих "мостов", что характерно для ряда предтромботических состояний (З.С. Баркаган и др., 1975, 1989). Кроме того, фактор Ха ретроградно активирует фактор VII в комплексе с ТF и Са++.
Далее будут рассмотрены отдельные этапы процесса свертывания крови и выделены показатели, имеющие наиболее важное клиническое значение. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 4:25 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 4:25 am Заголовок сообщения: |

|
|
1.2.1. Трансформация фибриногена в фибрин
Фибриноген (Фг; фактор I) - плазменный глобулярный гликопротеин, относящийся к белкам "острой фазы" и определяющий в значительной степени вязкость крови и плазмы, а также интенсивность агрегации тромбоцитов. Поэтому гирерфибриногенемия, являющаяся маркером явного или латентно текущего воспалительного процесса, либо наличия опухоли или деструкции тканей (в том числе инфаркта миокарда), сама по себе является фактором высокого тромбогенного риска и нуждается в устранении.
Конечная фаза свертывания крови, как известно, характеризуется трансформацией растворенного в плазме фибриногена в волокна фибрина, которые образуют основной каркас сгустка крови.
Эта фаза может быть подразделена на следующие три этапа:
Этап 1. Отщепление тромбином от молекулы фибриногена двух фибринопептидов А и двух фибринопептидов В, в результате чего образуются фибрин-мономеры (ФМ) с четырьмя свободными связями. Повышение содержания в плазме фибринопептидов А и В служит маркером активации свертывающей системы крови и тромбинемии.
Этап 2 (неферментный). Процесс полимеризации фибрин-мономеров вначале в димеры, затем - в тетрамеры и более крупные олигомеры, остающиеся еще в растворенном виде, но по мере дальнейшего укрупнения трансформирующиеся в волокна фибрина. Регуляция полимеризации фибрин-мономеров изучена далеко не полностью, но показано, что ряд пептидов и отрицательно заряженных мукополисахаридов (в том числе и гепарин) тормозят этот процесс (Д.М. Зубаиров, 1990; А.Ш. Бышевский и др., 1990).
Этап 3. Образование сгустка фибрина и стабилизация последнего фактором ХIIIа, благодаря чему фибрин становится нерастворимым в 5М мочевине. Активация фактора XIII также осуществляется тромбином (фактором IIа) в присутствии иoнов Са.
Конечный этап свертывания в лабораторных условиях воспроизводится тромбиновым тестом, а также пробами с тромбиноподобными ферментами змеиных ядов - анцистроном, рептилазой, арвином и др. Но последние в отличие от тромбина отщепляют от фибриногена только пептиды А и не активируют фактор XIII.
Удлинение времени свертывания в этих тестах может быть связано с гипофибриногенемией, молекулярными аномалиями фибриногена, действием гепарина или других веществ, обладающих антитромбиновым эффектом (гирудин и др.), или больших количеств продуктов фибринолиза (ПДФ). Тесты с коагулазами змеиных ядов не чувствительны к гепарину, но отражают другие, перечисленные выше влияния, что используется в диагностике.
При ДВС-синдромах и тромбоэмболиях содержание в плазме фибрин-мономера и олигомеров фибрина, обозначаемых так же как "растворимые фибринмономерные комплексы" (РФМК), резко возрастает. Их выявление в повышенном количестве имеет важное значение для диагностики тромбинемии и внутрисосудистого свертывания крови. Для этого используются тесты паракоагуляции - этаноловый, протамин-сульфатный и наиболее информативный из них - ортофенантролиновый, позволяющий определять количество РФМК в плазме крови (В.А. Елыкомов, А.П. Момот, 1987), методы определения фибрин-мономера по агглютинации нагруженных фибриногеном латексных частиц или эритроцитов, либо иммунологически тестами определения концентрации фибринопептида А. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 4:31 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 4:31 am Заголовок сообщения: |

|
|
1.2.2. Трансформация протромбина в тромбин
Этот процесс реализуется протромбиназным комплексом (комплексом 3, см. схему), в котором активным началом является фактор Ха, а акцелератором процесса - фактор Vа. При этом, от протромбина отщепляются фрагменты 1+2, после чего одноцепочная молекула протромбина трансформируется вначале в мейзотромбин, а затем в двухцепочный активный фермент-тромбин (фактор IIа). Активация фактора X на фосфолипидной мембране резко ускоряется Ас-глобулином (фактором V), который, как и фактор VIII, активируется по механизму обратной связи первыми небольшими дозами тромбина.
1.2.3. Начальная фаза свертывания крови
Как видно из схемы на рис.6, активация фактора X может осуществляться двумя путями - по внешнему (быстрому) и внутреннему (медленному) механизмам.
Внешний механизм запускается поступлением в кровь тканевого тромбопластина. В лабораторных условиях этот механизм воспроизводится протромбиновым (тромбопластиновым) тестом, при выполнении которого к цитратной плазме добавляют тканевый тромбопластин и хлорид кальция, после чего регистрируют время образования сгустка.
Удлинение протромбинового времени при нормальных показаниях тромбинового теста (см. выше) может быть обусловлено дефицитом факторов VII, X, V и II, причем нарушение только в этом тесте при нормальных показаниях всех других коагуляционных проб может быть связано только с дефицитом фактора VII.
Тормозится этот процесс ингибитором тканевого пути свертывания, обозначаемого как ТFРI, а также наличием в плазме некоторых антифосфолипидных антител (волчаночного антикоагулянта), для чего используется тест с разведенным (ослабленным) тромбопластином.
Внутренний механизм начального этапа свертывания крови реализуется цепной (каскадной) реакцией, в которой, как видно из схемы на рис.6, последовательно активируются факторы XII, XI, IX и VIII. В отличие от внешнего механизма в данном процессе не
участвуют тканевый тромбопластин и фактор VII. Активация по этому пути инициируется контактом крови (плазмы) с субэндотелием, особенно коллагеном, что ведет к образованию активного "контактного" комплекса, в который входят фактор ХIIа-калликреин-фактор ХIа. В пробирочных условиях запуск этого механизма осуществляется контактом крови (плазмы) с чужеродной поверхностью - стеклом, каолином, целитом и др.
Оценивается свертывание по внутреннему механизму путем определения общего времени свертывания крови (от момента извлечения ее из сосудистого русла до образования сгустка в пробирке; норма - 5-10 минут), но намного более точно - по активированному частичному (парциальному) тромбопластиновому времени (АЧТВ или АПТВ).
В этом тесте усиливаются и стандартизируются контактная (добавлением каолина) и фосфолипидная (добавлением кефалина) активация процесса свертывания (норма при использовании разных реагентов чаще всего - 30-40 секунд).
Этой же цели служит так называемый "аутокоагуляционный тест" (АКТ), отражающий кинетику образования и инактивации тромбина в исследуемой плазме при стандартизированной гемолизатом эритроцитов контактной и фосфолипидной активации процесса свертывания (В.П. Балуда и др., 1980; Л.З. Баркаган, 1993).
Из приведенных данных следует, что с помощью трех указанных выше базисных коагуляционных тестов (тромбинового, протромбинового и АЧТВ) можно получить информацию о состоянии всех основных звеньев процесса свертывания крови, определить, в каком из них имеется нарушение у исследуемого больного. Дополняются эти тесты определением содержания фибриногена в исследуемой плазме, для чего лучше пользоваться коагулометрическим методом (по А. Сlauss, 1957) либо методом взвешивания подсушенных сгустков по Р.А. Рутберг (см. В.П. Балуда и др., 1980). |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 4:53 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 4:53 am Заголовок сообщения: |

|
|
1.2.4. Оценка результатов общих коагуляционных тестов
Все перечисленные исследования, как и последующие определения активности отдельных факторов свертывания крови, могут выполняться как вручную, так и более легко, быстро и точно - на коагулометрах разной конструкции (оптических, шариковых и др.). При этом, важно, чтобы определения выполнялись с помощью высокостандартизированных реагентов, прошедших предварительное тестирование на эталонных образцах плазмы при сравнении с международными эталонами тромбопластина и факторов свертывания крови. Из отечественных реагентов такой стандартизации подвергаются диагностикумы, выпускаемые фирмой "Технлогия-стандарт" (Барнаул).
В табл. 2 приведены данные о том, в каких сочетаниях нарушаются показания базисных коагуляционных тестов при дефиците различных факторов свертывания крови и при действии антикоагулянтов.
Дефицитные факторы
и эффекты антикоагулянтов | Замедление свертывания | | В АЧТВ и АКТ | В протромбиновом тесте | В тромбиновом тесте | | XII* | + | - | - | | XI | + | - | - | | Прекалликреин* | + | - | - | | ВМ кининоген* | + | - | - | | IX | + | - | - | | VIII | + | - | - | | Фактор Виллебранда | Часто + | - | - | | VII | - | + | - | | V | + | + | - | | X | + | + | - | | II* | + | + | - | | I | + | + | + | | XIII* | - | - | - | | Действие гепарина | + | + | + | | Действие кумаринов | + | + | - | | Примечание: * - отмечены крайне редкие формы патологии |
Анализ их позволяет сделать следующие заключения:
- Удлинение протромбинового времени (ПВ) при нормальных показаниях АПТВ и тромбинового времени (ТВ) свойственно только дефициту фактора VII.
- Нарушение показаний АПТВ (АКТ) при нормальных ПВ и ТВ наблюдается только при дефиците или ингибиции факторов VIII, IX, XI и XII, а также прекалликреина и высокомолекулярного кининогена. Из этих форм патологии наиболее часты (более 97%) и сопровождаются выраженной кровоточивостью дефицит и/или ингибиция факторов VIII и IX, что характерно для гемофилии А и В, а также дефицит фактора Виллебранда, более редко - появление в крови прежде здоровых людей иммунных ингибиторов фактора VIII.
- Замедление свертывания только в тромбиновом тесте имеет место при дисфибриногенемиях и нарушениях полимеризации фибрин-мономеров (в том числе и под влиянием ПДФ).
- Замедление свертывания как в АПТВ, так и в протромбиновом тесте при нормальном ТВ и уровне фибриногена в плазме более 1,0 г/л наблюдается при дефиците факторов Х, V и II, а также при воздействии непрямых антикоагулянтов (кумаринов, варфарина, фенилина и др.).
- Нарушение показаний всех трех базисных тестов наблюдается при гепаринотерапии, глубокой гипофибриногенемии, воздействии на систему свертывания продуктов фибринолиза, лечении активаторами фибринолиза.
Дальнейшая дифференцировка нарушений свертываемости крови проводится с помощью коррекционных проб и тестов смешивания, а также пробами с коагулазами змеиных ядов. В табл. 3-6 представлены данные о принципах, лежащих в основе выполнения этих тестов, чтении их результатов.

Примечание. Плюс означает, что фактор имеется, минус - отсутствует
1 - Адсорбцию производят либо бария сульфатом из оксалатной плазмы (ВаSО4 - плазма), либо гелем гидроокиси алюминия из цитратной плазмы (Аl(ОН)3-плазма).
2 - Предварительно хранится 2-4 дня при +4°С.
3 - Фильтрацию производят через два асбестовых фильтра (фильтры Зейца) - с 20% (верхний фильтр) и 30% (нижний фильтр) содержанием асбеста либо через удвоенный или утроенный соответственно 30 и 20% фильтры.
4 - Используется плазма цыплят или утят в возрасте до 3-4 дней.

 |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 5:25 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 5:25 am Заголовок сообщения: |

|
|
1.2.5. Витамин К-зависимые факторы свертывания крови
При многих видах патологии гемостаза наблюдается сопряженный дефицит синтезируемых в гепатоцитах витамин K-зависимых факторов (факторов VII, IX, X и II). Это может быть связано либо с тяжелым поражением паренхимы печени (в этих случаях одновременно выявляются гипоальбуминемия и дефицит фактора V), либо с нарушением гамма-карбоксилирования этих факторов под влиянием витамин К-зависимой карбоксилазы. В результате этого не подвергшиеся карбоксилированию факторы свертывания утрачивают способность соединяться с Са,sup>++ и участвовать в процессе свертывания крови, но иммунологически они обнаруживаются в крови в нормальном количестве в виде некарбоксилированных и нефункционирующих молекул, обозначаемых в литературе аббревиатурой РIVКА.
Такое нарушение карбоксилирования витамин К-зависимых факторов свертывания крови со значительно более высоким уровнем в плазме РIVКА наблюдается у новорожденных (с максимальным снижением протромбинового индекса на 3-5 день после рождения), а также при приеме антикоагулянтов непрямого действия (кумаринов, варфарина, фенилина и др.).
Помимо указанных выше факторов свертывания крови, в гепатоцитах при участии витамин К-зависимого гамма-карбоксилирования синтезируются два важнейших физиологических антикоагулянта - протеины С и S, синтез которых нарушается под влиянием тех же причин, что и синтез факторов VII, X, IX и II. К этой же группе относится протеин Z, функция которого еще точно не определена.
1.2.6. Неферментные факторы свертывания крови
В эту группу, помимо фибриногена, входят два важных акцелератора процесса свертывания крови - факторы VIII и V. Оба они весьма лабильны, плохо сохраняются в донорской плазме при ее инкубации без глубокого замораживания, имеют короткую продолжительность жизни в крови реципиента после трансфузий.
Фактор VIII представлен комплексом белковых молекул, выполняющих в гемостазе различную функцию. В него входят следующие компоненты: - Фактор VIII:С - коагуляционный компонент фактора, ускоряющий активацию фактора IX, с которым в присутствии Са++ образует комплекс на фосфолипидной матрице. Этот компонент обозначается как "антигемофильный глобулин", поскольку его дефицит лежит в основе гемофилии А. Однако снижение активности фактора VIII:С, связанное с ослаблением стимуляции его синтеза, наблюдается и при ряде форм болезни Виллебранда.
- Фактор Виллебранда (VIII:ФВ) - крупномолекулярный белок, контролирующий тромбоцитарный гемостаз и необходимый, в частности, для адгезии тромбоцитов к субэндотелию. Вместе с тем, VIII:ФВ является стимулятором синтеза фактора VIII:С, в силу чего при его дефиците или аномалиях содержание в плазме фактора VIII:С часто снижается. Вследствие этих особенностей при дефиците фактора Виллебранда наблюдаются в разных сочетаниях удлинение времени "капиллярного" кровотечения в пробах Дьюка, Айви, А.С. Шитиковой и др., нарушение коллаген- и ристомицин-агрегации тромбоцитов и более или менее выраженное снижение активности фактора VIII:С.
С фактором VIII:ФВ связан главный антигенный маркер этого фактора, обозначаемый как фактор VIII:Аг. Вторым антигеном этого фактора является сам белок VIII:С. Поэтому при иммунизации возможно появление двух видов антител к фактору VIII: анти-VIII:С и анти-VIIIР:Аг.
Имеются данные, что в состав фактора VIII входят еще два компонента, один из которых является низкомолекулярным кофактором белка VIII:С (З.С. Баркаган и др., 1969).
Синтез фактора VIII:С контролируется геном, локализующимся в Х-хромосоме, а факторов VIII:ФВ и VIIIР:Аг - в аутосомах (МсКusick, 1994; Sау, 1995).
Фактор V - синтезируемый гепатоцитами глобулин, акцелерирующий активацию фактора X в протромбиназном комплексе (см. схему свертывания). В отличие от других факторов, синтезируемых гепатоцитами, фактор V не зависит от обеспеченности организма витамином К. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 5:31 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 5:31 am Заголовок сообщения: |

|
|
1.3. Особенности функционирования коагуляционного каскада
Важной особенностью этого многоступенчатого ферментного процесса является то, что в нем от момента запуска до конечного этапа происходит интенсивное наращивание числа последовательно активируемых молекул. Так, например, одна молекула фактора IХа активирует несколько десятков молекул фактора X, а одна молекула Ха - множество молекул фактора II (протромбина). Поэтому этот процесс может быть уподобен скорее не водопаду (сравнение с последним часто фигурирует в литературе), а камнепаду, при котором сорвавшийся с горы один камень вовлекает в процесс обвала все большее и большее число нижележащих камней.
Как уже указывалось выше, в системе свертывания действуют силы ретроградной активации, примером тому может служить активирующее действие фактора Ха на комплекс "тканевый тромбопластин-фактор VII".
Далее будут рассмотрены и механизмы самоторможения системы. |
|
| Вернуться к началу |
|
 |
blizzard
Site Admin

Зарегистрирован: 27.03.2008
Сообщения: 8675
Откуда: Москва
Благодарности: 1443
|
 Добавлено: Вс Янв 11, 2009 5:56 am Заголовок сообщения: Добавлено: Вс Янв 11, 2009 5:56 am Заголовок сообщения: |

|
|
1.4. Противосвертывающие механизмы
В системе свертывания крови действуют силы не только самоускорения, но и последующего самоторможения, в силу чего факторы свертывания крови и их метаболиты приобретают антикоагулянтные свойства. Так, например, фибрин связывает и инактивирует большие количества тромбина и фактора Ха. Тормозят конечный этап свертывания и продукты расщепления фибриногена плазмином (см. раздел 1.5). Точно так же препятствуют свертыванию метафакторы Vа и ХIа.
Рассматривая эту трансформацию факторов свертывания в вещества, противодействующие гемокоагуляции и тромбообразованию, нельзя не обратить особого внимания на свойство тромбина превращаться из основного фактора свертывания крови в активатора важнейшего противосвертывающего механизма.
На уровне организма этот феномен впервые был выявлен и изучен Б.А. Кудряшовым и его школой (1975). Однако один из важнейших молекулярных механизмов этого феномена, обозначаемый в современной литературе как "тромбиновый парадокс" Griffin, 1995), был расшифрован много позже. Выяснилось, что очень значительная часть тромбина, образующегося при активации свертывающей системы крови, связывается с тромбомодулином сосудистой стенки и утрачивает при этом способность вызывать образование фибрина и активировать фактор XIII. Вместе с тем, такой заблокированный тромбомодулином тромбин сохраняет способность активировать систему важнейших антикоагулянтов - протеинов С и S, вызывать через них активацию фибринолиза. Поэтому тромбин трансформируется в мощный противотромботический агент.
В процессе постоянной слабой активации свертывающей системы крови, носящей в организме перманентный характер (Д.М. Зубаиров, 1978), фактически весь образующийся тромбин связывается с тромбомодулином и, не вызывая гемокоагуляции, поддерживает в активном состоянии указанный выше противосвертывающий механизм и жидкое состояние циркулирующей крови Griffin, 1995; Seligson, 1996).
Важнейшую роль в поддержании жидкого состояния крови играет группа первичных физиологических антикоагулянтов (табл.7).
Таблица 7. Основные первичные физиологические антикоагулянты
| Наименование антикоагулянта | Механизмы действия | | Антитромбин III (АТIII) | Прогрессивно действующий ингибитор тромбина, фактора Ха и в меньшей степени других ферментных факторов свертывания. Плазменный кофактор гепарина | | Гепарин | Сульфатированный полисахарид, образующий комплексы с АТ III, переводящий последний в быстродействующий антикоагулянт | | Кофактор гепарина II | Слабый антикоагулянт, действие которого выявляется в присутствии гепарина после удаления из плазмы АТ III | | Протеин С | Витамин К-зависимая серин-амидаза, инактивирующая факторы VIIIа и Vа; эндогенный активатор плазминогена. Активируется тромбином и комплексом "тромбомодулин-тромбин" | | Протеин S | Витамин К-зависимый кофактор протеина С | | Тромбомодулин | Гликопротеин, фиксированный на цитоплазматической мембране эндотелия. Связывает и инактивирует тромбин, но не ослабляет его активирующего действия на протеин С | | Ингибитор тканевого пути свертывания (ТFРI) | Ингибитор комплекса "тканевый фактор-фактор VIIа-фактор Ха-Са++" | | "Контактные ингибиторы" (фосфолипидный, плацентарный) | Нарушают активацию внутреннего механизма свертывания (комплексы факторов XII и XI) | | Антитромбопластины альфа2-макроглобулин | Ингибиторы комплекса факторов III - VIIа. Слабый ингибитор тромбина, плазмина, калликреина | | Альфа1-антитрипсин I | Ингибитор тромбина, факторов IХа, ХIа, ХIIа, плазмина | | Ингибитор комплемента I (Анти-СI) | То же | | Ингибиторы полимеризации фибрин-мономеров | Тормозят образование фибрина |
Представленная на рис.7 схема иллюстрирует механизмы действия основных первичных физиологических антикоагулянтов.
 |
|
| Вернуться к началу |
|
 |
|
|
Вы не можете начинать темы
Вы не можете отвечать на сообщения
Вы не можете редактировать свои сообщения
Вы не можете удалять свои сообщения
Вы не можете голосовать в опросах
|
| |
|
|
|
Код для вставки ссылки на форум и сайт:

|
|
|
Информация, представленная на данном форуме,
предназначена исключительно для образовательных целей,
не должна использоваться для
самостоятельной диагностики и лечения, и не может служить заменой очной консультации врача.
Администрация сайта не несёт ответственности за результаты, полученные в ходе самолечения с
использованием материалов форума.
Перепечатка информационных материалов форума разрешается при условии размещения
активной ссылки на оригинальный материал.
(c) 2008 blizzard.
Все права защищены и охраняются законом.
|

|
|














